烷烴化學性質|| 烷烴類是什么?
一系列飽和脂肪烴(如甲烷、乙烷等)中的任何一種,此類化合物是石油的主要成分。 烷烴是飽和烴,是只有碳-碳單鍵的鏈狀烴。 烷烴的化學性質在 NCERT 化學主題中得到了很好的定義。
它們是簡單的有機化合物。 在烷烴中,氫原子數達到大值。 分子中的每個碳原子都是sp3雜化。 簡單的烷烴是甲烷。
同時,烷烴也是許多元素的飽和氫化物的總稱。
分類為氫化物后綴和系統
單核及其名稱
“烷烴”(-ane 后綴)實際上不僅指碳的飽和氫化物,還可以指所有母體分子均不含不飽和鍵的分子氫化物。 單核氫化物直接以“元素+烷烴”命名。
一些不同的可變元素氫化物使用相同的烷烴名稱,非標準鍵數氫化物以“λ”為前綴來區分。 從上表我們可以知道一般飽和烷烴的名稱。
標準鍵數:鹵族1、氧族2、氮族3、碳族4、硼族3。
例子:
C6H5-SH5——苯基-λ?-硫烷
(C6H5)3PH2——三苯基-λ?-正膦
烷烴的命名
從對應的數字開始,卡賓不引入碳元素前綴,非碳水化合物必須添加核元素前綴。
例子:
H2N-NH2——疊氮
HS-SH4-SH——2λ?-丙硫烷
PH2(PH)15PH2-十七烷
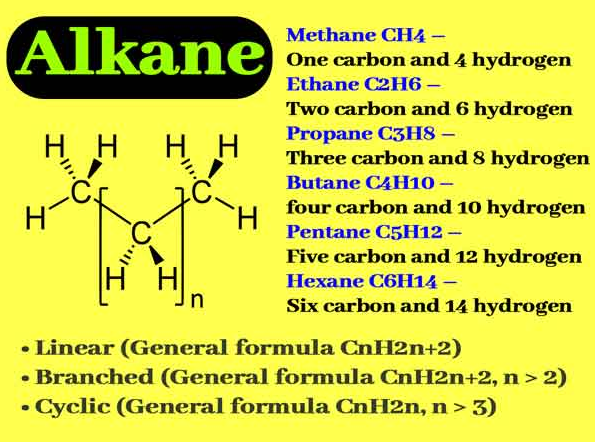
線性己烷命名法
當母原子被另一個原子取代時,名稱應由雜原子的相應前綴修飾。當烷烴的骨架鏈電子被其他雜原子隨機占據時,原名稱用雜原子前綴修飾,但雜原子的總數應計入骨架鏈的總電子數中。
例子:
SiH3 OSiH2O (SiH2)2 OSiH2 SiH3 ——2,4,7-三氧雜環己烷
如果雜原子和主鏈原子在鏈上交替出現,且鏈兩端的元素相同,則稱鏈段原子為雜原子。 鏈原子的數量不用說。
例子:
SiH3 NHSiH3 – 二硅二硅氮烷
NH2 (SiH2 NH)3 SiH2 NH2——(C19H27NO)
烷烴:
在烷烴中,每個碳原子都是四價的,只有碳-碳單鍵和烴單鍵。使用 sp3 雜化軌道,它與周圍的 4 個碳或氫原子形成牢固的 σ 鍵。
與1、2、3、4個碳相連的碳原子分別稱為伯、仲、叔、季碳;伯碳、仲碳和叔碳上的氫原子
它們被稱為伯氫、仲氫和叔氫。
為了小化鍵的排斥力,連接到相同碳的四個原子形成一個四面體。甲烷是標準正四面體,鍵角為109°28′。
理論上,由于烷烴穩定的結構,所有的烷烴都可以是穩定的。
然而,自然界中的烷烴多不超過50個碳,豐富的烷烴是甲烷。
由于烷烴中的碳原子可以按規律隨機排列,烷烴的結構可以寫成無數種。直鏈烷烴是基本的結構,理論上,這條鏈可以無限延伸。烷烴的化學性質
可以在直鏈上產生支鏈,這無疑增加了烷烴的數量。
因此,從一個4碳烷烴開始,同一種烷烴的分子式可以表示多個結構。這種現象稱為異構現象。隨著碳數的增加,異構體的數量將迅速增加。
烷烴也可能發生光學異構現象。當一個碳原子連接的四個原子團不同時,這種碳稱為手性碳,這種物質具有光學活性。
烷烴中失去一個氫原子的剩余部分稱為烷基,一般用R-表示。因此,烷烴也可用通式RH表示。
烷烴初是使用習慣命名法命名的。然而,這種命名法難以用于具有許多碳數和許多異構體的烷烴。因此建議命名派生,都被認為是甲烷烷烴的衍生物,例如異丁烷,稱為 2-甲基丙烷。
烷烴應用:
由于烷烴生產成本較高(通常烯烴用于催化加氫),烷烴不是工業生產的,而是直接從石油中提取的。 由于烷烴不易反應,在工業上不用作基礎化工原料。
烷烴的作用主要是制造燃料。 天然氣和沼氣(主要由甲烷組成)是近廣泛使用的清潔能源。
由于大部分烷烴來自石油,因此必須經過分餾過程才能獲得各種不同用途的烷烴。


